Theo Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA), lô thuốc bị thu hồi mang số A1540076 có túi truyền được dán nhãn là Levetiracetam trong dung dịch natri clorid 0,82%, hàm lượng 500 mg/100 mL, tuy nhiên, thông tin được ghi trên bao bì nhôm bên ngoài lại ghi đúng là Levetiracetam trong dung dịch natri clorid 0,75%, hàm lượng 1.000 mg/100 mL.
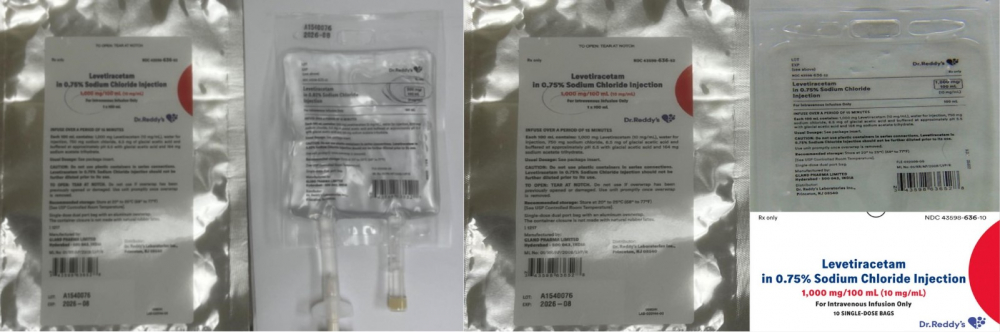
Theo cơ quan chức năng, sai sót này có thể khiến bệnh nhân vô tình nhận gấp đôi liều lượng so với mong muốn, dẫn đến các tác dụng phụ nghiêm trọng như phản ứng quá mẫn, tổn thương gan, độc tính trên máu, buồn ngủ, mệt mỏi, chóng mặt, khó phối hợp vận động, kích động, trầm cảm, suy hô hấp và hôn mê.
Đặc biệt, những bệnh nhân sử dụng liều cao Levetiracetam qua đường truyền tĩnh mạch nhanh để điều trị trạng thái động kinh có nguy cơ gặp tác dụng phụ nghiêm trọng nhất. Tuy nhiên, đến thời điểm hiện tại, Dr. Reddy’s chưa ghi nhận trường hợp nào bị ảnh hưởng bởi sự cố này.

Được biết, lô thuốc Levetiracetam nằm trong diện thu hồi được sử dụng như liệu pháp bổ trợ trong điều trị các loại động kinh ở người trưởng thành (từ 16 tuổi trở lên) khi không thể dùng đường uống, bao gồm: Động kinh cục bộ; Động kinh cơ giật ở bệnh nhân mắc động kinh cơ giật tuổi vị thành niên; Động kinh toàn thể co cứng - co giật.
Sản phẩm được đóng gói trong túi truyền liều đơn, có bao nhôm bên ngoài, 10 túi truyền được đóng trong một hộp. Lô thuốc bị thu hồi đã được phân phối trên toàn nước Mỹ từ ngày 4/11/2024 đến ngày 6/11/2024 đến các nhà bán buôn.
Hiện, Dr. Reddy’s Laboratories đang thông báo đến các nhà phân phối và khách hàng để thu hồi lô sản phẩm bị ảnh hưởng. Các nhà bán buôn, nhà thuốc, bệnh viện có lô thuốc này cần ngừng sử dụng, phân phối và cách ly sản phẩm để trả lại hoặc thay thế. Những đơn vị đã phân phối tiếp sản phẩm cần thông báo đến các cơ sở liên quan. Nếu gặp bất kỳ vấn đề sức khỏe nào liên quan đến sản phẩm này, người tiêu dùng nên tham khảo ý kiến bác sĩ.
Quỳnh Trang












