Cục Quản lý Dược (Bộ Y tế) vừa ra quyết định xử phạt vi phạm hành chính Công ty Cổ phần 23 tháng 9 (số 11 Tân Hóa, Phường 14, Quận 6, TP.HCM) về hành vi sản xuất thuốc vi phạm chất lượng mức độ 2 đối với thuốc Batiwell, dùng hỗ trợ điều trị nhiễm khuẩn đường hô hấp, giúp long đờm.
Cụ thể, Công ty Cổ phần 23 tháng 9 do ông Hồ Văn Thành làm Chủ tịch Hội đồng quản trị đã có hành vi sản xuất thuốc Batiwell, số giấy đăng ký lưu hành VD-31011-18, số lô 00121, ngày sản xuất 8/3/2021, hạn dùng 8/3/2024 vi phạm chất lượng mức độ 2 theo quy định của pháp luật.
Theo Cục Quản lý Dược, Công ty Cổ phần 23 tháng 9 đã vi phạm quy định tại điểm b khoản 4 Điều 57 Nghị định số 117/2020/NĐ-CP ngày 28.9.2020 của Chính phủ quy định xử phạt vi phạm hành chính trong lĩnh vực y tế.
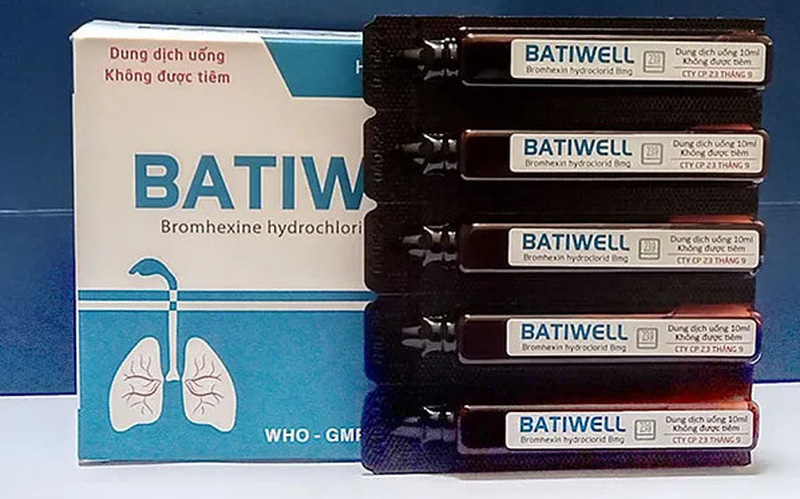
Bộ Y tế cho biết thuốc Batiwell do Công ty Cổ phần 23 tháng 9 sản xuất không đảm bảo hiệu quả điều trị và có nguy cơ không an toàn cho người sử dụng.
Do đó, Cục Quản lý Dược quyết định xử phạt Công ty Cổ phần 23 tháng 9 với số tiền 70 triệu đồng và buộc đơn vị này tiêu hủy toàn bộ số thuốc vi phạm chất lượng. Ngoài ra, Cục yêu cầu Công ty tiến hành thu hồi số thuốc vi phạm chất lượng, thực hiện biện pháp khắc phục hậu quả và báo cáo kết quả thực hiện về Cục Quản lý Dược trong vòng 30 ngày kể từ ngày ban hành Quyết định.
Trước đó, Cục Quản lý Dược đã thông báo thu hồi toàn quốc lô thuốc Dung dịch uống Batiwell (Bromhexin hydroclorid 0,8mg/ml), Số GĐKLH: VD-31011-18, Số kiểm soát: 00121, NSX: 8/3/2021, HD: 8/3/2024 do Công ty cổ phần 23 tháng 9 sản xuất.
Theo đó, Cục yêu cầu Công ty cổ phần 23 tháng 9 phối hợp với nhà phân phối gửi thông báo tới các cơ sở bán buôn, bán lẻ, sử dụng thuốc và tiến hành thu hồi toàn bộ lô thuốc không đạt tiêu chuẩn chất lượng nêu trên.
Đồng thời gửi báo cáo thu hồi về Cục Quản lý Dược trong vòng 18 ngày, hồ sơ thu hồi bao gồm số lượng sản xuất, ngày sản xuất, số lượng thu hồi, các bằng chứng về việc thực hiện thu hồi tại các cơ sở bán buôn, bán lẻ, sử dụng đã mua thuốc theo quy định.
Cục Quản lý Dược đề nghị Sở Y tế các tỉnh thành phố, Y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thu hồi lô thuốc không đạt chất lượng nêu trên; công bố thông tin về quyết định thu hồi thuốc trên Trang thông tin điện tử của Sở; kiểm tra và giám sát các đơn vị thực hiện thông báo này; xử lý những đơn vị vi phạm theo quy định hiện hành; báo cáo về Cục Quản lý Dược và các cơ quan chức năng có liên quan.
Giao Sở Y tế TP.HCM kiểm tra và giám sát Công ty 23 tháng 9 thực hiện việc thu hồi và xử lý thuốc bị thu hồi theo quy định.
SHTT